5月20日是“国际临床试验日”(International Clinical Trials Day)。这一纪念日设立的初衷是纪念一位伟大的军医,一起来看看是怎样的故事……
国际临床试验日的由来
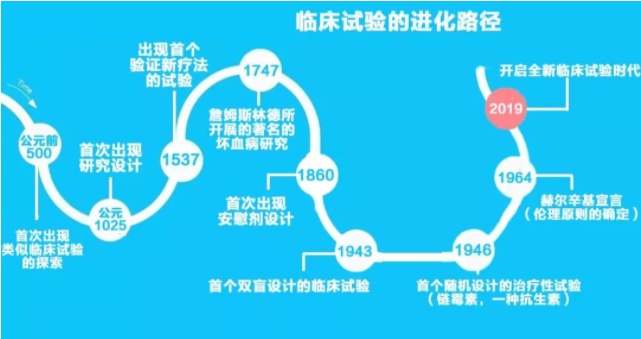
1747年5月20日,苏格兰军医詹姆斯林德设计开展了著名的“坏血病临床试验”,具有随机、对照、前瞻的特点,开启了现代临床试验的新篇章。为纪念这一历史性事件,欧洲临床研究协作组联合美国和加拿大,将每年的5月20日定为国际临床试验日。2005年5月20日成为了第一个“国际临床试验日”。此后,每年的这个日子,国际上都会举行一系列的学术、科普推广活动,以此来提高公众对临床试验的认知。

临床试验是什么?
根据我国2020年《药物临床试验质量管理规范》(GCP),临床试验是指以人体(患者或健康受试者)为对象的试验,意在发现或验证某种试验药物的临床医学、药理学以及其他药效学作用、不良反应,或者试验药物的吸收、分布、代谢和排泄,以确定药物的疗效与安全性的系统性试验。
以新药为例,一款新药在实现临床广泛应用之前,需要经历重重考验:在研发阶段,涉及靶点的确定、模型的建立、先导化合物的发现和优化。由此而得出的“临床前候选化合物”,会进入开发阶段,包括临床前试验、临床试验注册申报,临床试验和新药申请。在这期间,临床试验是新药开发中的必要环节,同时也是“上市成败”的关键步骤。任何新药必须经过上市前临床试验阶段,才可能被批准上市用于广泛人群。
新药临床试验如何开展?
在我国,新药临床试验必须参照《药物临床试验质量管理规范》执行,需在获得国家药监局批准并进行登记与信息公示。
通常,新药临床研究分为四个阶段——Ⅰ、Ⅱ、Ⅲ、Ⅳ期,各期临床试验数据和报告结果都需要有科学性、真实性和可靠性。

源自《药物临床试验质量管理规范》
临床试验中要保护受试者权益
受试者是参与临床试验的受试对象(包括患者和健康志愿者),他们的权益和安全是临床试验考虑的首要因素。伦理委员会和知情同意书是保护受试者强有力的两大武器。受试者有权充分了解试验目的、试验过程与期限、检查操作、预期可能的受益和风险,同时可以随时退出试验。参与临床试验受益和风险是什么呢?以肿瘤临床试验为例,受试者参与国内PD-1药品三期试验,由于临床试验期间产生的相关费用由申办方按照法规要求承担,部分受试者不但能有效治疗癌症,还能减少治疗费用,减轻家庭负担。然而,临床试验受试者也可能会经历一些治疗的副反应,而且要投入更多精力往来医院,配合研究机构采血样,接受特定检查等等。所以,临床试验中一定要对受试者进性充分知情,让受试者根据自身情况做出选择。
深圳市中医院新药临床试验开展状况
我院早在2011年就被国家药监局(原国家食品药品监督管理局)认定为国家药物临床试验机构,并根据国家药品监督管理局综合司《关于做好药物临床试验机构备案工作的通知》(药监综药注(2019)100号)的相关要求,于2020年11月完成了8个专业组药物临床试验机构备案工作。截止目前,我院已承担近40项Ⅱ-Ⅳ期新药临床试验项目。此外,非注册类科研项目近年也在逐年增加。有意在我院开展新药临床试验项目的申办方企业,可在医院官网“科研平台”版块查询相关流程。有意开展科研临床研究的院内研究人员,可在院内OA科研“下载专栏-科教科”版块查询开展流程。
最后,在第17个国际临床试验日到来之际,我们呼吁所有临床研究工作者,积极参与临床试验研究,为推动医疗健康事业发展、为更多新药上市做出一份贡献!
供稿来源:深圳市中医院科教科刘玉



